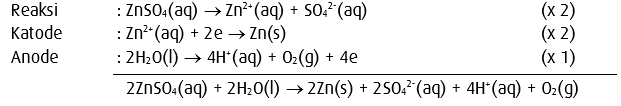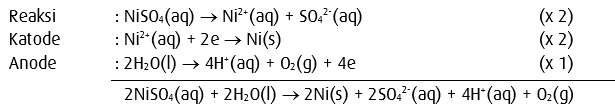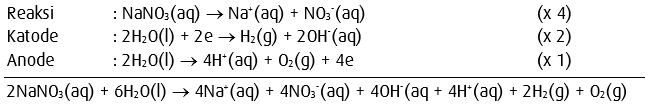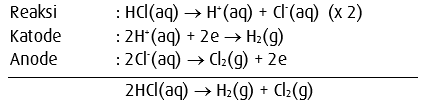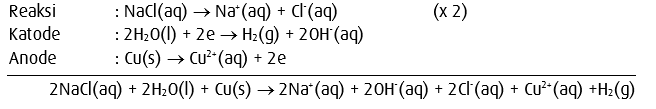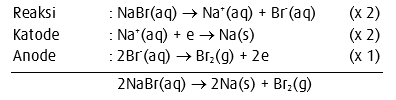Reaksi Kimia yang Terjadi Dalam Sel Elektrolisis
Reaksi kimia yang terjadi dalam sel elektrolisis perlu memperhatikan ketentuan-ketantuan berikut.
“Dalam reaksi elektrolisis terjadi persaingan antarspesi (ion atau molekul) untuk mengalami reaksi reduksi atau reaksi oksidasi. Setiap zat yang mempunyai kemampuan reduksi besar (potensial reduksi besar) akan mengalami reaksi reduksi dan setiap zat yang mempunyai kemampuan oksidasi besar (potensial oksidasi besar) akan mengalami reaksi oksidasi.”
Elektrolisis Larutan
Pada elektrolisis larutan, zat-zat (unsur-unsur) yang terlibat dalam reaksi, selain kation, anion, dan pelarut (air) harus diperhatikan juga elektrodenya. Untuk mempermudah menyelesaikan reaksi elektrolisis, perhatikan dua cara penyelesaian berikut ini.
Skema reaksi-reaksi elektrolisis larutan
Katode:
perhatikan kation :
- H+ ; Kation H+ tereduksi menurut:
2H+(aq) + 2e → H2(g) - Logam :
- logam golongan IA, IIA, Al, dan Mn, logam-logam yang tidak tereduksi, yang tereduksi adalah air :
2H2O(l) + 2e → H2(g) + 2OH–(g) - logam-logam lainnya, maka logam lain tersebut tereduksi :
Lx+(aq) + xe → L(s)
- logam golongan IA, IIA, Al, dan Mn, logam-logam yang tidak tereduksi, yang tereduksi adalah air :
Anode:
- Anode inert (Pt, Au, C):
- OH- : anion OH- teroksidasi : 4OH–(aq) → 2 H2O(l) + O2(g) + 4e
- Sisa asam :
- Beroksigen (asam oksi), maka air yang teroksidasi:
2H2O(l) → 4H+(aq) + O2(g) + 4e - Tanpa oksigen, maka sisa asam itu teroksidasi:
2Cl–(aq) → Cl2(g) + 2e2
Br–(aq) → Br2(g) + 2e
- Beroksigen (asam oksi), maka air yang teroksidasi:
- anode tidak inert maka teroksidasi :
L(s) → Lx+(aq) + xe
Diselesaikan dengan bantuan tabel potensial reduksi dan potensial oksidasi
Elektrolisis larutan :
- Katode : spesi yang mengalami reduksi di katode adalah spesi yang mempunyai potensial reduksi besar.
- Anode : spesi yang mengalami oksidasi di anode adalah spesi yang mempunyai potensial oksidasi yang besar.
Contoh
1. Elektrolisis larutan CuSO4(aq) dengan elektrode Pt.
2. Elektrolisis larutan CuSO4 dengan elektrode Cu
Ternyata dari kedua contoh di atas, cara a lebih mudah daripada cara b.3. Elektrolisis larutan ZnSO4 dengan elektrode Pt
4. Elektrolisis larutan NiSO4 dengan elektrode grafit (C)
5. Elektrolisis larutan NaNO3 dengan elektrode Pt
6. Elektrolisis larutan HCl dengan elektrode C
7. Elektrolisis larutan NaCl dengan elektrode Cu
Elektrolisis Leburan/Lelehan/Cairan
Pada elektrolisis larutan hanya kation, anion, dan elektrode yang terlibat dalam reaksi karena senyawa ionik tidak mengandung air (H2O).
contoh
1.Elektrolisis cairan KCl dengan elektrode Pt.
2. Elektrolisis lelehan NaBr dengan elektrode C.